La investigación puede tener aplicaciones en la ingeniería naval o en la predicción de erupciones volcánicas.

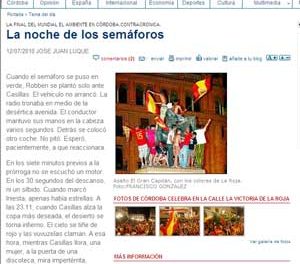
Científicos de la Universidad Carlos III de Madrid han desvelado el fenómeno que explica la rápida transformación de estado líquido a espumoso de la cerveza tras recibir un impacto. Foto: Felix
Científicos de la Universidad Carlos III de Madrid han desvelado el fenómeno físico que explica la rápida transformación de estado líquido a espumoso de la cerveza tras un impacto. Esta investigación, que puede sonar a chiste, puede encontrar sin embargo numerosas aplicaciones en ingeniería naval o en estudios relativos a la predicción de gases en erupciones volcánicas.
La investigación surgió, como no podía ser de otro modo, tras la barra de un bar al ver cómo se derramaba la espuma de una cerveza después de que alguien hiciera la broma de golpear el cuello de una botella con la base de otra, confiesan los investigadores.
“Cada uno de los que estábamos allí comenzamos a lanzar hipótesis y teorías acerca de la causa de ese fenómeno, pero no nos convenció ninguna y decidimos llevarlo al laboratorio para investigarlo mediante experimentos controlados y en condiciones bien definidas para analizar qué fenómenos físicos hay detrás de la aparición de esta espuma”, comenta Javier Rodríguez, profesor del departamento de Ingeniería Térmica y de Fluidos de la UC3M, que ha presentado un avance de los resultados en la última conferencia anual sobre mecánica de fluidos de la Sociedad de Física Americana, la más prestigiosa del mundo.
El estudio, realizado en colaboración con el Instituto Jean le Rond D’Alembert (una unidad de investigación mixta del CNRS y la Universidad Pierre et Marie Curie, en Francia), detalla en tres fases lo que ocurre después de que la botella reciba el golpe:
- En primer lugar, aparecen ondas de expansión y compresión que avanzan por dentro del líquido y producen la rotura de las cavidades de gas (las burbujas) en el fondo de la botella.
- Después, se forman pequeñas bolitas de espuma porque las burbujas se rompen en otras aún más pequeñas.
- Y por último (dado que pesan menos que el líquido que las rodea), esas burbujas suben tan rápidamente que el resultado final se asemeja a una explosión.
La espuma aparece porque en las bebidas gaseosas se pone más dióxido de carbono (CO2) de lo que el agua (componente principal) es capaz de mantener en disolución. “Habitualmente el CO2 escapa muy despacio. Pero esa cadena de fenómenos provocados por el golpe en la botella multiplican la pérdida de gas por un factor tremendamente alto: una botella puede perder en segundos el gas que le costaría horas perder si simplemente la dejáramos abierta sobre la mesa”, explica Javier Rodríguez.
Para demostrar la validez de su teoría, los investigadores idearon un sistema para estudiar a cámara lenta el fenómeno. En primer lugar, apuntaron con un láser pulsado de alta energía hacia la base de la botella para provocar la aparición de una burbuja. A continuación, dieron un golpe en el cuello y grabaron todo con una cámara de alta velocidad que les permite obtener más de 50.000 fotogramas por segundo. Gracias a ello han sido capaces de describir al detalle el proceso que está detrás de esta reacción en cadena: la cavitación. Se trata de un efecto hidrodinámico similar a la ebullición (en lo que se refiere a la formación de burbujas), pero que aparece cuando desciende la presión en un líquido.
Esta investigación puede tener aplicaciones muy serias, como la predicción de la cantidad de gases que se producen tras la erupción de un volcán. Comprender mejor el fenómeno de la cavitación puede ayudar a mejorar el diseño de las hélices de los barcos (que están muy expuestas a la erosión provocada por las burbujas), a optimizar la protección de las estructuras frente a explosiones o determinadas ondas de choque, o favorecer las reacciones químicas por medio de la implosión de burbujas, señalan los investigadores.
Fuente: UC3M.